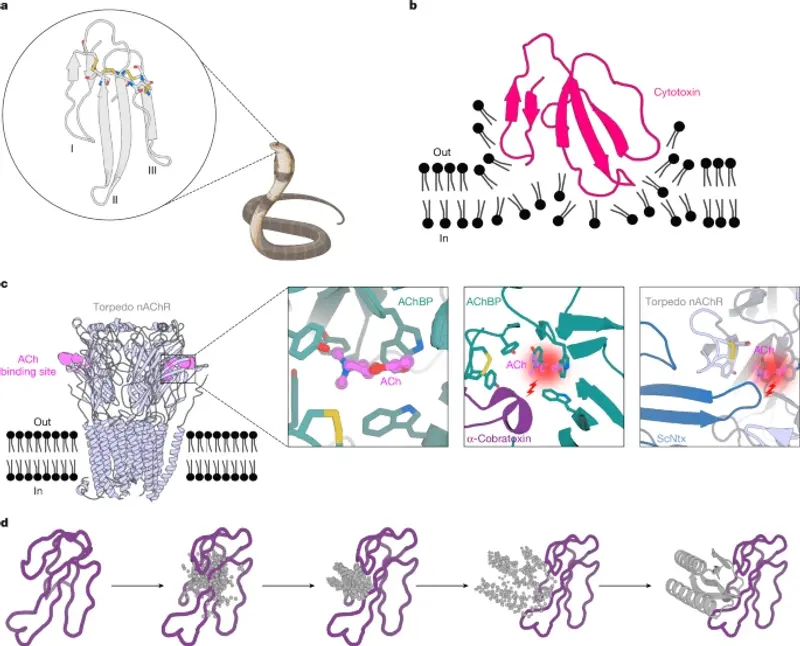
在《自然》杂志上发表的一项新研究中,研究人员利用人工智能(AI)设计了全新的蛋白质,这些蛋白质能够抑制蛇毒中的某些毒素。这项研究由华盛顿大学的大卫·贝克(David Baker)领导的团队完成,展示了 AI 工具如何帮助研究人员应对原本困难或不可能解决的挑战。
蛇毒的复杂性与现有治疗方法的局限
蛇毒包含一系列复杂的毒素,其中大部分是蛋白质,它们对被咬伤的生物发起多方面的攻击。目前的主要治疗方法是使用与这些毒素结合的抗体混合物,这些抗体是通过将亚致死量的蛇毒蛋白注射到动物体内产生的。然而,抗蛇毒血清通常需要冷藏,保质期也很短,且生产过程复杂,需要定期给新动物注射蛇毒并从它们体内纯化更多的抗体。
新研究的目标与意义
这项新研究的目标是设计更小、更稳定的蛋白质,以执行与抗蛇毒血清相同的功能。这些蛋白质可以在细菌中生产,可能生成一种不需要冷藏的抗蛇毒血清,这对于许多发生在农村或荒野地区的蛇咬伤事件尤为重要。
研究团队专注于一种特定的有毒蛇毒蛋白:三指毒素(three-finger toxins),因其蛋白质折叠成的物理结构而得名。三指毒素是黑曼巴蛇、太攀蛇和眼镜蛇等臭名昭著的蛇毒的主要成分。尽管它们的体积相对较小,但三指毒素家族的不同成员能够产生两种不同类型的损害:一组通过破坏细胞膜导致细胞普遍中毒,而另一组则能够阻断神经递质的受体。
利用 AI 设计蛋白质
阻断神经毒素
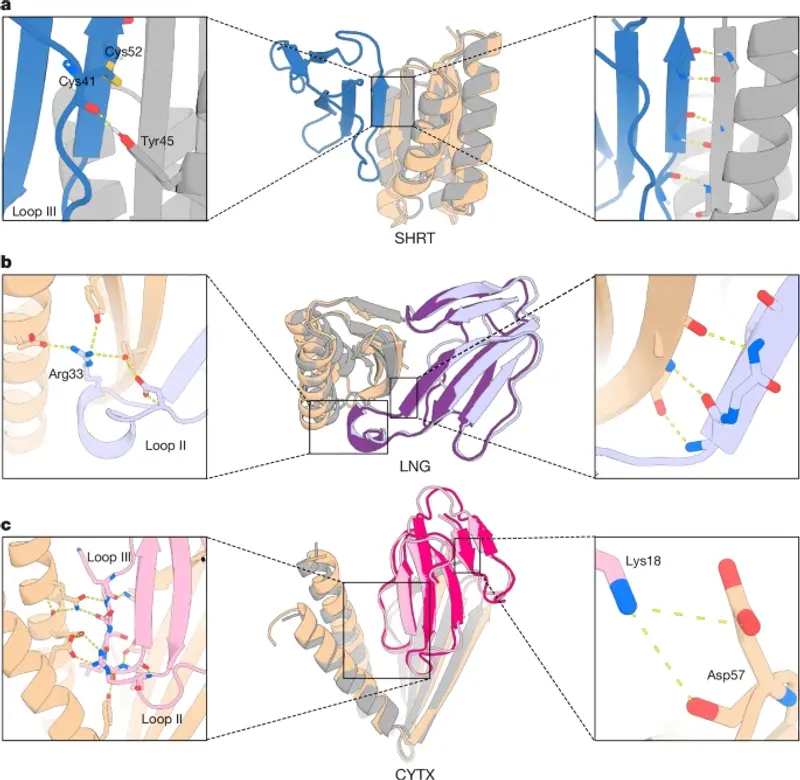
神经毒性三指蛋白是较大蛋白质家族的一个亚组,专门结合并阻断乙酰胆碱(一种主要神经递质)的受体。研究人员利用 AI 软件包 RFdiffusion 设计出与特定化学物质互补的蛋白质结构,识别出可以与三指毒素中的链边缘对齐的新链。随后,使用 ProteinMPNN 识别全长蛋白质的氨基酸序列,这些蛋白质将形成新识别的链。
研究人员将三指毒素和一组新设计的蛋白质输入 DeepMind 的 AlfaFold2 和 Rosetta 蛋白质结构软件,估计它们之间的相互作用强度。测试了 44 种计算机设计的蛋白质与三指毒素的相互作用能力,并选择了相互作用最强的蛋白质进行进一步研究。通过 RFDiffusion 提出可能更有效结合的蛋白质变体,约 15% 的建议确实与毒素的相互作用更强。最终,研究人员在细菌中制作了毒素和最强的抑制剂,并获得了它们相互作用的结构,证实了软件的预测非常准确。
阻断细胞毒素
另一组三指毒素可以通过破坏细胞膜直接杀死细胞。研究人员创建了与三指毒素强烈相互作用的抑制剂,并可能抑制其活性。然而,当在实际小鼠身上测试时,这些抑制剂并未减少由三指毒素引起的皮肤损伤的大小。这可能表明我们尚未完全理解这些蛋白质如何破坏细胞膜,并且可能错误地瞄准了抑制的区域。因此,研究人员停止了对这种抑制剂的测试。
概念验证与未来展望
尽管这些研究成功,这项工作主要是概念验证。蛇毒通常含有多种毒素,而这些实验仅针对其中的两种。此外,所生产的蛋白质之所以有效,是因为它们具有高度特异性。但这种特异性意味着,针对眼镜蛇毒液中的蛋白质设计的抑制剂可能对更远缘蛇类的毒液无效。
尽管如此,这项工作表明,AI 工具确实可以极大地扩展我们在干预生物学方面的选择。如果没有这些工具,这项工作很可能在第一步就陷入困境,因为几乎不可能通过推理来识别可能与这种毒素相互作用的蛋白质结构。而完善任何初步想法可能需要数月到数年的艰苦工作。这项研究展示了 AI 在生物医学研究中的巨大潜力,为未来的研究提供了新的方向和方法。(地址)